Остеопластические материалы
Натуральный костный материал InterOss со скидкой 5%
При единовременном заказе 10 штук

Остеопластические материалы
Костнопластические материалы для замещения костной ткани.Костнозамещающие гранулы BioOst Xenograft






BioOST
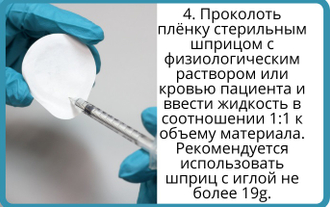
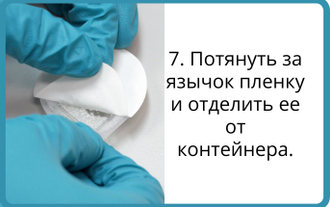
Все остеопластические материалы серии «bioOST» представляют собой очищенную стерильную костную ткань крупного рогатого скота, прошедшего тщательные ветеринарные обследования. Глубокая очистка матрикса проводится по уникальной технологии с применением сверхкритической флюидной экстракции. Сверхкритическая жидкость, способная хорошо растворять липиды, обеспечивает удаление всех неколлагеновых белков, протеолипидов, клеток костного мозга и жиров, а также гарантирует отсутствие в готовом остеопластическом материале бактерий, вирусов или прионов. При этом в очищенном таким образом ксеногенном матриксе сохраняются природный коллаген и естественные факторы роста, которые являются опорным белком и стимулирующими регенерацию молекулами, гарантирующими физиологическое восстановление недостающей кости. Различные виды обработки сырья позволяют предложить биоматериалы с нужными характеристиками, а отказ от применения для очистки агрессивных химических реагентов позволяет избежать нежелательных реакций от остатков веществ.
В зависимости от остаточного содержания неорганической фазы, матрикс «bioOST» выпускается деминерализованным (содержащим коллаген) и не имеющим органическую составляющую. При деминерализации открываются зашитые гидроксиапатитом белки фактора роста, что обеспечивает хорошую остеоиндуцируемость матрикса. В результате минерально-коллагеновый матрикс демонстрирует как остеокондуктивные, так и остеоиндуктивные свойства, что позволяет добиться максимально качественных результатов при замещении дефектов.
Прошедший термическую переработку ксеногенный материал не содержит уже в своем составе коллаген. Такой матрикс представляет собой керамизированный гидроксиаппатит животного происхождения (аморфные гранулы фосфата кальция и биологического апатита в естественных пропорциях). Этот ксеноматериал обладает отличной остеокондуктивностью и достаточно высокой прочностью. При использовании в качестве остеопластического материала позволяет достичь формирования прогнозируемого обьема новообразованноого регенерата.
Резюме
Проведена сравнительная оценка эффективности хирургического лечения 63 человек с околокорневыми кистами челюстей с заполнением костной пазухи остеопластическим материалом Osteo Biol (группа сравнения) и BioOst (исследуемая). Результаты, полученные у исследуемой группы, заявляют о преобладании скорости процессов остеогенеза над быстротой резорбции, что в свою очередь, характеризует остеозамещающие гранулы BioOst как отвечающие современным требованиям, предъявляемым к таким материалам.
Введение
Проблема регенерации кости является одной из актуальных проблем в современной дентальной хирургии. Дефицит челюстной ткани может возникнуть в результате различных причин, например, после удаления зубов, хронических периапикальных очагов и внутрикостных новообразований, травматических повреждений лицевого скелета.
Известно, что восстановление объемных внутрикостных пустот нередко занимает продолжительное время (до 4–5 лет) и не всегда происходит в полном объеме. Наличие сопутствующей патологии может способствовать еще большему увеличению сроков регенерации.
На сегодняшний день теоретически обоснована и клинически доказана возможность управления процессом остеорепарации посредством применения различных по строению оптимизаторов костяной ткани. В связи с этим остеопластические материалы нашли широкое применение в клинике хирургической стоматологии и челюстно-лицевой хирургии.
Используемые сегодня материалы обладают выраженным остеорегенераторным потенциалом, аналогичны костям человека по морфологическому строению, биосовместимы и неиммуногенны. Однако на практике использование остеопластических графтов далеко не всегда приводит к ожидаемому положительному результату. В ряде случаев развиваются такие нежелательные явления, как отторжение имплантата или образование замыкательной фиброзной капсулы вокруг него.
В связи с этим перед клиницистами возникает проблема выбора остеопластического материала, способного обеспечить положительный результат лечения и не требующего больших финансовых вложений. По-прежнему сохраняет актуальность вопрос экономической доступности реконструктивных стоматологических операций. При этом важная роль отводится разработке и внедрению в клиническую практику бюджетных отечественных новинок для полноценной регенерации объема и структуры ткани челюстей, обеспечивающих стабильный результат. С этих позиций перспективным может быть использование отечественной остеопластической крошки BioOst.
BioOst Xenograft представляют собой обработанную физико-химическим способом костную ткань крупного рогатого скота. Ксенографты Bio-Ost химически, иммунологически и структурно совместимы с костью человека. Метод стерилизации матрикса — газовый (стерилизация оксидом этилена).
Цель исследования
Подтверждение рациональности употребления российского остеопластического графта BioOst Xenograft в дентальной хирургии.
Материал и методы
Нами проведено обследование и лечение 63 людей первого периода зрелого возраста (21–35 лет) с околокорневыми кистами челюстей. Выбор данной патологии обусловлен тем фактом, что стенки выемки, оставшейся после цистэктомии, являются инфицированными, что способствует развитию осложнений в послеоперационном периоде. Возрастной сегмент характеризуется прогрессивными процессами роста и формообразования костей.
Наиболее часто мы наблюдали локализацию кист в области резцов и клыков, что связано с желанием сохранить эти зубы.
В зависимости от метода лечения больные были разделены на две категории. В первой группе (сравнения — 31 человек) полость заполнялась остеопластическими гранулами Osteo Biol, во второй (исследуемой) — 32 участника — BioOst (Россия). Цистэктомия проводилась с сохранением анатомической формы зуба.
Критериями включения больных в исследование были информированное согласие на участие в исследовании и отсутствие сопутствующей патологии. Формирование клинических сегментов проводилось в соответствии с принципами простой рандомизации.
Эффективность лечения оценивали по динамике клинических проявлений.
Активность репаративных процессов в костяном изъяне оценивали по данным ортопантомограмм визуально, а также посредством компьютерного продукта Photoshop 7.0 при этом оценивали оптическую плотность (показатель минеральной насыщенности, ПМН) дефекта и показатель резорбции. Периодичность клинических наблюдения составила 3, 6 и 9 месяцев.
Статистическая обработка полученных данных проводилась непосредственно из общей матрицы данных Excel 10.0 с привлечением возможностей программы Statistica 6. Группировка вариационных рядов и их обработка проводились в соответствии с рекомендациями.
Математический анализ состоял из последовательно проводимых статистических методов. Вариационно-статистический ряд включал определение следующих вариационно-статистических элементов: M, m, t, p, где M — средняя арифметическая, m — ошибка средней арифметической, t — коэффициент достоверности. Различие средних арифметических считали значимым при р < 0,05.
Результаты исследования и их обсуждение
На момент обращения общее состояние у всех больных оценивалось как удовлетворительное. Проявлений местного воспалительного процесса не наблюдалось. Показатель минеральной насыщенности (ПМН) интактной кости составил 158,32 ± 2,19 у. е., костного дефекта — 78,27 ± 2,17 у. е. (p< 0,001), показатель резорбции (Пр) составил 44,88 ± 2,21%.
Послеоперационный период протекал гладко, заживление раны первичным натяжением наблюдалось у всех на 10–12-е сутки.
Через три месяца после операции у пяти больных группы сравнения отмечались чувство дискомфорта и небольшая болезненность при простукивании зубов и пальпации слизистой оболочки в месте хирургического вмешательства. При анализе рентгенограмм отмечалось снижение прозрачности тени костяной полости с четко выраженными отграниченными участками (фото 1а). ПМН составил 98,47 ± 2,23 у. е. (p < 0,001), резорбция — 39,54 ± 1,19% (p< 0,05). Люди из исследуемой гр. жалоб не предъявляли, никаких признаков воспалительного процесса в месте операции не было обнаружено. Анализ рентгенограмм показал равномерное снижение прозрачности тени дефекта умеренной плотности на всем его протяжении (фото 1б). ПМН составил 127,59 ± 2,34 у. е. (p < 0,001), Пр — 32,47 ± 2,19% (p< 0,001).
Таким образом, уже через 3 месяца после операции у 16,1 % участников сегмента сравнения наметилась тенденция к отторжению имплантата, в то время как у больных основного - превалировали процессы остеогенеза.
Через полгода после имплантации у пяти людей из гр. сравнения клинически видимой положительной динамики не наблюдалось. Неприятные ощущения и незначительная боль при перкуссии зубов и прощупывании слизистой оболочки в области операционного вмешательства сохранялись. Анализ рентгенограмм свидетельствовал о снижении прозрачности костной выемки, однако ее границы четко прослеживались, в верхнем отделе отмечались две тени повышенной плотности. ПМН увеличился относительно аналогичного показателя трехмесячной давности (108,54 ± 2,15 у. е.; p < 0,01), а Пp стабилизировался на уровне предыдущего этапа наблюдения (38,75 ± 2,16 %; p> 0,05;), фото 2а.
Остальные пациенты этой группы жалоб не предъявляли. Рентгенологически отмечалось равномерное снижение прозрачности тени костяного изъяна.
Больные основного сегмента жалоб не озвучивали, клинических признаков воспаления или отторжения гранул в области имплантации не наблюдалось. Анализ рентгенограмм показал равномерное увеличение плотности тени повреждения на всем его протяжении (фото 2б). ПМН составил 133,52 ± 2,16 у. е. (p < 0,05), Пp оставался таким же, как на предыдущем этапе наблюдения (31,61 ± 2,32%; p> 0,05).
Таким образом, динамика клинико-рентгенологических показателей свидетельствовала о том, что у пациентов группы сравнения тенденция к отторжению имплантата стала более выраженной, у участников основной гр. сохранилась активность остеогенеза.
Через 9 месяцев после операции у этих пятерых (16,2%) клинически отмечалось формирование свищевого хода в проекции костного дефекта со скудным гнойно-геморрагическим отделяемым. На рентгенограмме отмечалось отграничение имплантата от стенок полости (фото 3а).
У больных основной группы клинически местных признаков воспалительного процесса не наблюдалось. Анализ рентгенограмм свидетельствовал об усилении плотности тени, даже с признаками формирования костяного рисунка (фото 3б). ПМН составил 140,54 ± 2,17 у. е. (p < 0,05), Пp не имел статистически значимой разницы относительно показателя предыдущего этапа наблюдения (30,22 ± 1,16%; p> 0,05).
Таким образом, показатели, полученные у исследуемых основного сегмента, свидетельствуют о превосходстве скорости остеогенеза над быстротой процессов резорбции, что дает понимание о полном соответствии остеозамещающих гранул BioOst Xenograft тем показателям и качествам, которые требуются от подобных разработок.
Ю.В. Ефимов, Д.В. Стоматов, Е.Ю. Ефимова, А.В. Стоматов, Д.В. Смоленцев, И.В. Долгова, П.В. Киреев.
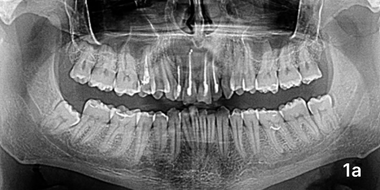
Ортопантомограмма пациента М., группа сравнения, область резцов, 3месяца от операции.
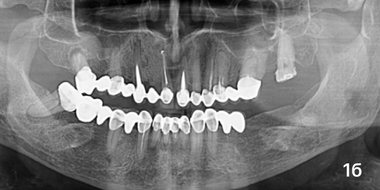
Ортопантомограмма пациента К, основная гр, область 1.3, 3мес после операции.
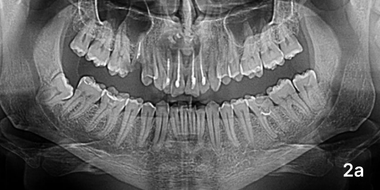
Пациент М, гр сравнения, 6 месяцев спустя.
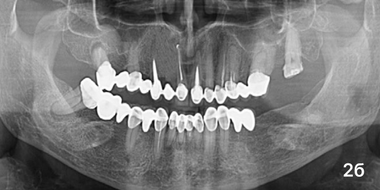
Пациент К, основная гр, через 6мес.
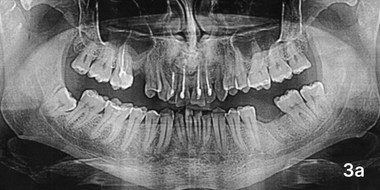
Пациент М, спустя 9 месяцев после операции.
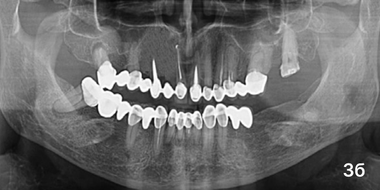
Пациент К, через 9месяцев от операции.

