Коллагеновые мембраны
Натуральный барьерный материал для НКР Creos Xenoprotect со скидкой 5%
При единовременном заказе 10 штук.
Резорбируемые мембраны для хирургической стоматологии.
Коллагеновые мембраны bioPlate разработаны для применения в челюстно-лицевой хирургии, хирургической стоматологии, имплантологии и пародонтологии и отвечают потребностям различных стоматологических показаний. Мембраны БиоПлейт дают возможность выполнить пластику любого дефекта, даже в сложных клинических ситуациях, в стоматологии используются для исправления дефектов и восстановления объема костной и мягких тканей, слизистой разной локализации и этиологии.Резюме: Авторами данной работы представлены результаты тестирования по свободной гетеротрансплантации коллагеновых резорбируемых мембран, используемых для направленной тканевой регенерации. На основании результатов проведенных испытаний исследуемые изделия можно рекомендовать для дальнейшего изучения в апробации на крупных животных в условиях ортотопической имплантации.
Актуальность исследования: Проблема восстановления объема костных конструкций давно является сферой фундаментальных и клинических изысканий. Локальный дефицит объема и высоты костей альвеолярного отростка и базального отдела челюстей имеет различную этиологию. Причинные факторы этого процесса представлены в широком диапазоне, это врожденная патология, последствия травмы, одонтогенные воспаления, хирургическое устранение новообразований. Бурное развитие дентальной имплантологии в последние годы обусловлено постоянно растущим спросом на данный вид стоматологической помощи.
Восстановление дефектов пародонта, мягких и твердых тканей челюстно-лицевой области решают как с помощью разработок новых методик реконструктивных операций, так и с использованием новых материалов, восполняющих утраченный объем. По происхождению эти биоматериалы делятся на три большие группы: аутотрансплантаты, то есть трансплантаты, которые берутся и используются у одной и той же особи; ксено- и аллотрансплантаты — наработки биологического происхождения, сырьем для которых являются животные и трупные исходники соответственно; имплантаты — продукты искусственного происхождения.
Несмотря на различный состав, все эти препараты должны соответствовать определенным требованиям: не вызывать токсических, аллергических и воспалительных реакций; не влиять на генный аппарат, хорошо интегрировать с тканями организма и не вызывать их резорбции; быть простыми в приготовлении и универсальными в употреблении а также относительно дешевыми в производстве. Помимо этого, мембраны должны быть применимы для культивирования на них культур клеток, в частности, аутологичных фибробластов.
Для эффективного использования различных видов имплантационных материалов необходимо иметь четкое представление о механизмах ответа организма на их внедрение и об их роли в репаративных процессах. Эффективным методом рассмотрения такого типа проблем является эксперимент на живых объектах.
Целью исследования являлось проведение сравнительного анализа биологического действия на живые ткани различных резорбируемых коллагеновых мембран при их гетеротопической имплантации. В связи с этим нами поставлены задачи проведения сравнительного гистологического анализа степени биоинтеграции и резорбции контрольного и опытных образцов, а также сравнительной гистологической оценки их биологического воздействия на организм подопытного существа.
Материалы и методы: Объектами испытания явились фрагменты следующих ксеноматериалов: Geistlich Bio-Gide, производитель Geistlich Pharma AG; стоматологическая коллагеновая мембрана BioPlate Membrane Barrier, производитель «Кардиоплант»— барьерная двухслойная биорезорбируемая, на основе перикарда крупного рогатого скота; cтоматологическая коллагеновая матрица BioPlate Membrane Matrix, производитель «Кардиоплант» — однослойная резорбируемая, на основе внеклеточного матрикса.
Для оценки местного действия биорезорбируемых коллагеновых мембран после их вживления использована модель подкожной подсадки исследуемых продуктов белым нелинейным крысам согласно ГОСТ ISO 10993–6–2011. В тестировании использованы три группы резорбируемых коллагеновых мембран. В качестве контроля служили экземпляры коллагеновой мембраны Bio-Gide как препарата, чьи свойства хорошо изучены.
Сравнительная характеристика исследуемых материалов приведена в табл. 1.
| Сравниваемый признак | Группа 1(контрольная): Bio-Gide |
Группа 2: Barrier | Группа 3: Matrix |
| Показания к применению | Регенерация костной и восстановление мягких конструкций |
Регенерация костной и восстановление мягких конструкций |
Регенерация костной и восстановление мягких конструкций |
| Происхождение | Изготовлена из мягкого соединительного покрова домашних животных | Изготовлена из мягкого соединительного покрова домашних животных |
Изготовлена из мягкого соединительного покрова домашних животных |
| Состав | Состоит из нативного, высокоочищенного коллагена |
Состоит из нативного, высокоочищенного коллагена |
Состоит из нативного, высокоочищенного коллагена |
| Наличие обработки сшивающим агентом | Не содержит химических сшивающих агентов |
Не содержит химических сшивающих агентов |
Не содержит химических сшивающих агентов |
| Наличие двухслойной структуры | + | + | - |
| Физические характеристики поверхности | Имеет 2 разнородные поверхности. Одна сторона гладкая и плотная, другая пористая (ворсистая) | Имеет 2 разнородные поверхности. Одна сторона гладкая и плотная, другая пористая (ворсистая) | Однородная (шероховатые пористые поверхности) |
| Степень гидрофильности (время полного пропитывания физраствором), с | 20 | 60 | 40 |
| Способность сохранения формы во влажном состоянии (время полного пропитывания физраствором), Max ++++ | ++ | ++ | + |
| Размеры, мм | 25×25; 30×40 | 15×20; 25×25; 30×40 | 25×25 |
| Вид упаковки | Двойной блистер | Двойной блистер | Двойной блистер |
| Метод стерилизации | Стерилизация γ-излучением | Стерилизация оксидом этилена | Стерилизация оксидом этилена |
По окончании апробации планируется провести гистологический анализ извлеченных из животных опытных моделей.
Имплантация резорбируемых коллагеновых мембран для изучения биологического действия на гетерототопической модели in vivo.
Из каждой группы биоимплантатов брали имплантаты размером 15 × 20 мм по 4 шт. Перед операцией их помещали в физиологический раствор не менее чем на пять минут.
Для испытания использовали четырех самцов белых нелинейных крыс массой 250–300 г, возрастом три месяца. Подопытных содержали в стандартных условиях вивария при постоянном доступе к воде и пище, 12-часовой смене светового режима. Операцию проводили под ингаляционным наркозом с диэтиловым эфиром (рис. 1).
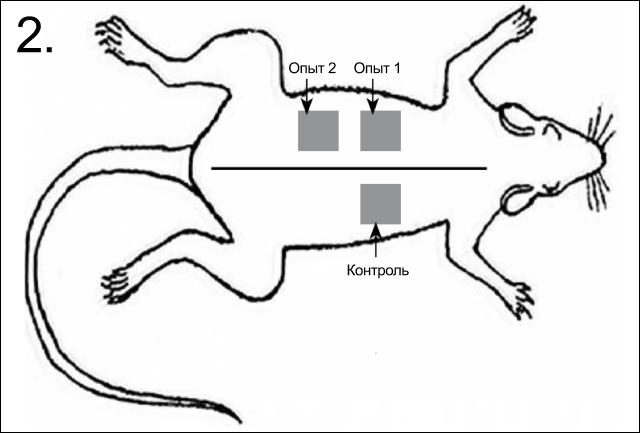
Резорбируемые мембраны имплантировали в карманы, сформированные вдоль средней линии спины (рис. 2).

Срок экспериментов: 4 и 12 недель. Дата внедрения образцов: 14.01.16. Дата выведения животных из эксперимента: 12.02.16 и 08.04.16.
После извлечения биоимпланты подвергались макроскопическому описанию и микроскопическому (гистологическому) исследованию для сравнения степени резорбции и биоинтеграции. Гистологические эспертизы проводились по общепринятой методике. Через 28 дней после подсадки экземпляры, извлеченные из животного, подвергались макроскопическому описанию.
В тестировании участвовали два самца нелинейных крыс. В первом подопытном не было обнаружено одного контрольного образца. Это возможно как следствие удаления имплантата самим грызуном. Во внешнем виде невооруженным глазом отличий между имплантами не наблюдалось. При тактильной диагностике фрагмент БиоПлейт Матрикс был мягче остальных, что является следствием разницы в структурах продуктов. При извлечении из подкожно-жировой клетчатки отмечалось покрытие мембраны тонкой пленкой соединительнотканных волокон реципиента.
Во втором животном найдены все экземпляры контроля и опытов. Во внешнем виде невооруженным глазом отличий между ними не замечались. При тактильном изучении bioPlate Matrix мягче остальных, что является следствием разных структур изучаемых изделий. При извлечении биоимплантатов из подкожно-жировой клетчатки установлено что они покрыты тонкой пленкой собственной фасциальной ткани грызуна. Четких границ образцов не прослеживалось.
Микроскопическое описание извлеченных мембран через четыре недели после имплантации.
Результаты микроскопического рассмотрения материалов через 28 дней после внедрения приведены в табл. 2.
| Контроль: Bio-Gide 1 | Bio-Gide 2 | Опыт 1: Barrier 1 | Barrier 2 | Опыт 2: Matrix 1 | Matrix 2 | |
| Биоинтеграция | Активная, врастание собственной соединительной ткани по краям и в центре |
По истечении 4 недель эксперимента не обнаружен |
Активная, врастание собственной соединительной ткани по краям и в центре |
Средняя, врастание собственных соединительных волокон только по краям |
Средняя, врастание собственных соединительных волокон только по краям |
Средняя, врастание собственных соединительных волокон только по краям |
| Васкуляризация (Max ++++) |
Выявляются новые кровеносные сосуды +++ | Выявляются новые кровеносные сосуды +++ | Выявляются новые кровеносные сосуды +++ | Выявляются новые кровеносные сосуды +++ | Выявляются новые кровеносные сосуды +++ | |
| Резорбция | Активная | Активная | Средняя | Средняя | Активная | |
| Наличие/отсутствие воспаления |
Слабо выражено, не по всем полям зрения | Слабо выражено, по всем полям зрения | Слабо выражено, по всем полям зрения (по краям) |
Слабо выражено, по всем полям зрения | Слабо выраженная, по всем полям зрения |
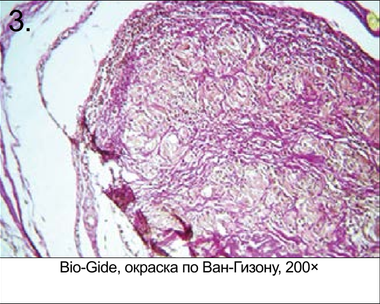
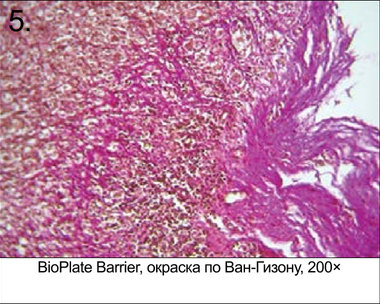
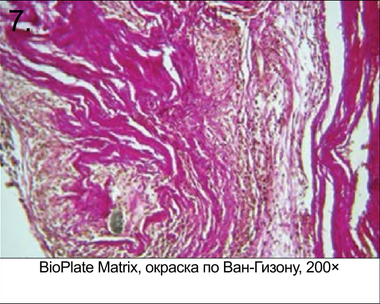
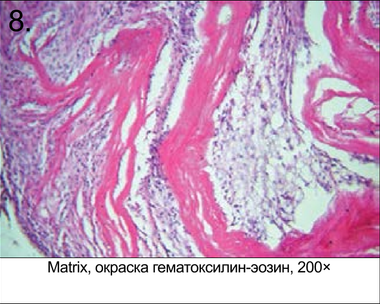
Микрофотографии гистологического испытания образцов, извлеченных через 4 нед. после имплантации (рис. 3–8)
Таким образом, по результатам гистологических анализов через один месяц после операции в подкожную жировую клетчатку лабораторным крысам, можно сделать вывод, что в состоянии мембраны Barrier нет значимых отличий от Bio-Gide. Через 28 дней подсадки на гетерототопической модели в группах Биоплейт Барьер и Био-гайд происходила активная биоинтеграция собственного фасциального покрова не только по краю изделий, но и в центре. В группе BioPlate Matrix через 4 нед. на гетеротопической модели биоинтеграция соединительнотканных волокон была наиболее выражена по краю имплантата. Во всех образцах появлялись новообразованные сосудистые системы в большом количестве. Выявлено начало активной биорезобции. Воспалительная реакция отмечена как слабовыраженная по всем полям зрения.
В последующем, после 12 недель внедрения, экземпляры, извлеченные из подопытных, также подвергались макроскопическому описанию.
В опытной работе участвовали две нелинейные крысы (самцы). У первого грызуна не обнаружено ни одного экспериментального образца. У второго самца определялись образчики и контроля и опыта 1. Во внешнем виде при исследовании невооруженным глазом отличий между мембранами не наблюдалось. При извлечении исследуемых фрагментов из подкожно-жировой клетчатки отмечалось полное их покрытие соединительной тканью реципиента. Биоимплантаты слабо просматривались через внеклеточный матрикс животного.
Остаток Биоплэйт Матрикс во втором грызуне также не был найден, что свидетельствует о его полной резорбции. Отличия в поведении коллагеновых мембран на разных особях являются следствием разного метаболизма у этих особей, так как в пределах одной особи их поведение не имеет явных отличий.
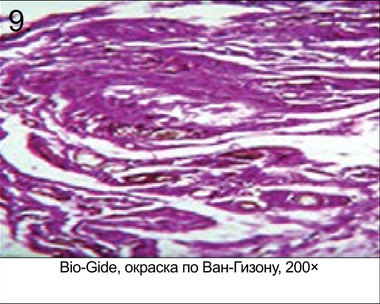
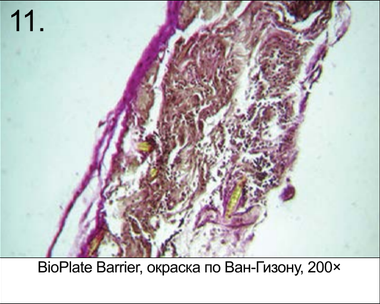
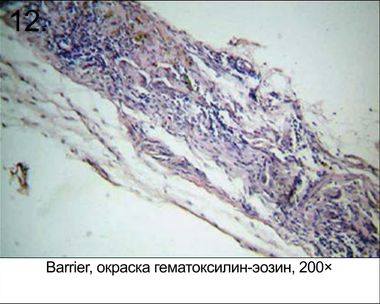
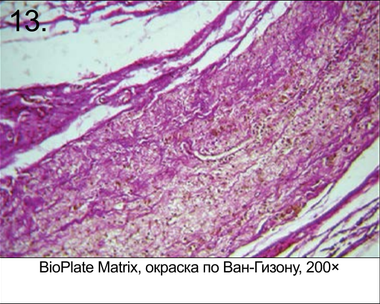
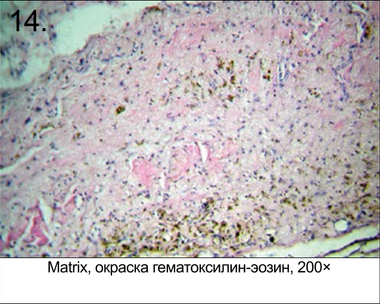
При извлечении определить четкие границы фрагментов не представлялось возможным. Диагностировать имплантаты можно было по более плотной и менее прозрачному коллагеновому покрову на месте вживления мембраны. Микрофотографии гистологического анализа извлеченных из крыс опытных моделей через 3 месяца после операции представлены на рис. 9–14. Таким образом, по результатам гистологических испытаний после 84 дней приживления можно сделать вывод, что в состоянии Биоплейт Барьер нет значимых отличий от состояния Био-Гайд. По истечении 12 нед. апробации экземпляры Matrix не найдены, что свидетельствует об их полной резобции.
Микроскопическое описание образцов, извлеченных из животного через 12 недель после имплантации.
Результаты микроскопического исследования через 84 дня после внедрения приведены в табл. 3
| Контроль: Bio-Gide 1 | Bio-Gide 2 | Опыт 1: Barrier 1 | Barrier 2 | Опыт 2: Matrix 1 | Matrix 2 | |
| Биоинтеграция | Средняя | По истечении 12 недель эксперимента не обнаружен |
Слабая | По истечении 12 нед. эксперимента не обнаружен |
По истечении 12 нед. эксперимента не обнаружен |
По истечении 12 нед. эксперимента не обнаружен |
| Васкуляризация (Max ++++) |
Встречаются групповые новообразованные кровеносные сосуды в соединительной аутоткани, окружающей образец, прорастание присутствует в виде единичных сосудов |
Встречаются единичные новообразованные кровеносные сосуды в соединительной аутоткани, окружающей образец; прорастание отсутствует |
||||
| Резорбция | По краям | По краям | ||||
| Наличие/отсутствие воспаления |
Воспаление минимальное |
Воспаление минимальное |
Выводы: Через один месяц после операции в состоянии мембраны Биоплэйт Барьер не установлено значимых отличий от Био-гайд. В группе Матрикс через 4 нед. приживления на гетеротопической модели биоинтеграция фасциальных коллагеновых волокон подопытных в отличие от Barrier и Bio-Gide была наиболее выраженна по краям. Во всех биоимплантах воспалительная реакция фиксирована как минимальная. Через 12 нед. в состоянии мембраны Барьер также не замечено значимых отличий от Био-гайд, воспалительная реакция также минимальная. Через 12 недель после подсадки экземпляры внеклеточного матрикса Matrix полностью резорбировались.
Таким образом, в результате проведенных доклинических исследований медицинского изделия BioPlate Barrier установлено, что испытанные единицы этого продукта биосовместимы с тканями реципиента, не вызывают воспалительных реакций, способны биоинтегрироваться в организм реципиента. На основании результатов проведенных опытных работ, а также с учетом результатов ранее проведенных технических испытаний и испытаний на биологическую безопасность, Биоплейт Барьер можно рекомендовать для дальнейшего изучения в проверках на крупных животных в условиях ортотопической имплантации.